INTRODUCCION
El organismo humano al igual que todos los organismos pluricelulares, posee mecanismos de defensa, ante cualquier agresión que afecte a sus tejidos. De esta forma las agresiones endógenas o exógenas provocan una cascada defensiva, donde la inmunidad innata, a través del proceso inflamatorio logra aislar la lesión, destruye el agente patógeno y repara el tejido con el fin de restaurar su funcionalidad y la del órgano afectado.1,3,5
Etimológicamente la palabra inflamación proviene del latín inflammatio, que quiere decir incendio o encender fuego; es así que se utilizaba esta palabra en la literatura médica para describir un órgano abultado, con aumento de calor local, que se comparaba con un proceso de combustión interna, dando lugar a lo que Celso describiera por primera vez los típicos signos cardinales de la inflamación, como son el rubor, calor, tumor y dolor.1,7
Por su parte John Hunter, cirujano escocés, en 1793 aclaró que la inflamación no es una enfermedad per se, sino una respuesta inespecífica que tiene un efecto saludable en el huésped. De no ser por el proceso inflamatorio las infecciones no podrían ser controladas, la curación y reparación de heridas sería imposible y los órganos lesionados no recuperarían su funcionalidad. De todas maneras el problema más representativo que se desencadena producto de la inflamación es que este mismo proceso de defensa se dirija hacia los agentes nocivos como a los que no lo son, de manera que resulte peligrosa al causar lesiones orgánicas graves como también reacciones de hipersensibilidad.1
DEFINICION
La inflamación es una reacción o proceso defensivo natural del sistema inmunológico del organismo como respuesta al daño causado a sus células y tejidos vascularizados por agentes lesivos como ser microorganismos, traumatismos, necrosis, agentes químicos o físicos, o reacciones inmunitarias entre otros. Esencialmente, es una respuesta protectora que surge con el fin de aislar, contener la lesión, destruir al agente agresor y posteriormente preparar al tejido dañado para su reparación, proceso que consta de cambios vasculares y celulares mediados por factores químicos que se manifiestan clínicamente, por datos que Aulo Cornelio Celso, enciclopedista médico romano, describió como signos cardinales que se presentan en todo proceso inflamatorio:1,2,3,5
SIGNOS CLINICOS
Los signos característicos de la inflamación son:
1) Calor: o aumento local de la temperatura secundario a vasodilatación, y aumento de consumo local de oxígeno.
2) Rubor: producido por el aumento de irrigación en la zona afectada, por incremento del flujo sanguíneo
3) Dolor: provocado por distensión de los tejidos y liberación de prostaglandinas como mediadores químicos.
4) Edema: resultante del aumento de la permeabilidad capilar y consiguiente sufusión de líquido en el tejido intersticial.
A estos signos Rudolf Virchow, médico alemán, les sumó un quinto signo clínico, functiolaesa, que es la pérdida de funcionalidad, resultante de la limitación a la que conduce la conjugación de los cuatro signos ya mencionados.1,8,9
CLASIFICACION
La clasificación de la inflamación se realiza tomando en cuenta el tiempo de duración, carácter del exudado, etiología, características morfológicas y localización:
1. Por la duración pueden ser:
a. Agudas: Este tipo de inflamación es una respuesta inmediata al agente agresor cuya finalidad es liberar mediadores de defensa del organismo en el área de la lesión cuyo comienzo es rápido y cursa una duración corta.
b. Crónicas: Es un proceso prolongado, existiendo en ese tiempo destrucción tisular, inflamación activa y un repetitivo intento de reparación.
2. Por el carácter del exudado pueden ser:
a. Trasudado: se caracteriza por la presencia de líquido extravascular con bajo contenido proteico, producto de un ligero cambio en la permeabilidad vascular.
b. Exudado: presencia de líquido inflamatorio extravascular con alto contenido proteico, lo cual denota bastante permeabilidad en los vasos sanguíneos.
3. Por la etiología, pueden ser:
a. Infecciosas: ya sea por bacterias, virus, parásitos o por toxinas microbianas
b. Traumáticas como golpes intensos con respuesta inmediata o tardía, como ocurre con los esguinces o higromas.
c. Térmicas resultantes de, quemaduras por calor o congelamiento.
d. Irradiaciones.
e. Por exposición a agentes químicos ambientales.
f. Necrosis tisular.
g. Presencia de cuerpos extraños como astillas.
h. Inmunitarias o reacciones de hipersensibilidad, a alergenos comunes o procesos colagenopáticos.
4. Por sus características morfológicas, pueden ser:
a. Serosa: por acúmulo de líquido tisular de bajo contenido proteico.
b. Fibrinosa: con presencia de exudado con grandes cantidades de fibrinógeno.
c. Supurativa o purulenta: se caracteriza por la producción de exudados purulentos que consta de leucocitos y células necróticas.
d. Abscesos: presenta tejido inflamatorio purulento acompañado de necrosis licuefactiva.
e. Úlceras: producidas por esfacelamiento de tejido necrótico inflamado.
5. Por su localización: Se dividen en:
a. Focales: producidas en zonas y órganos específicos, en cuyo caso se utiliza el sufijo -itis, por ejemplo faringitis, otitis, laringitis, conjuntivitis, peritonitis.
b. Diseminados: resultado de la propagación de procesos inflamatorios persistentes ya sea por vía canalicular, fistulización o metástasis.1,2,8
FISIOPATOLOGIA
La inflamación es un cuadro donde los cambios fisiopatológicos más sobresalientes son:
a) Cambio Vasculares:
En el proceso inflamatorio los vasos sanguíneos sufren cambios importantes en el flujo y calibre que posibilitan y maximizan la salida de proteínas y células plasmáticas desde la circulación hacia el foco inflamatorio. Uno de los primeros cambios vasculares es la vasodilatación, inducida por la histamina, producida por las células cebadas y el ácido nítrico, que actuarán sobre el músculo liso vascular, dilatándolo, con el consiguiente aumento de la permeabilidad microvascular, resultado de la combinación del aumento de la presión hidrostática y la disminución de la presión osmótica,lo que lleva a la salida de líquidos del espacio intravascular al extravascular con la formación de edema.
Estos cambios tienen como consecuencia la disminución de la velocidad sanguínea, que sumada a la pérdida de líquido intravascular, concentración de hematíes y aumento de la viscosidad de la sangre, da como resultado la éstasis, la cual es responsable de la marginación de los leucocitos, los cuales en condiciones normales circulan por el centro de los vasos. Simultáneamente se producen:
b) Cambios Celulares:
Los leucocitos deben viajar desde la luz de los vasos sanguíneos al sitio de la lesión y ejecutar ahí sus funciones de defensa, es decir, fagocitar al agente patógeno. A este proceso se le denomina extravasación y consta de tres etapas:
Marginación, rodadura y adhesión al endotelio.
Diapédesis.
Migración a los tejidos intersticiales.
Para que los leucocitos migren a través de las uniones interendoteliales hacia el sitio de la lesión siguen el curso de una locomoción orientada por un gradiente químico, que es la quimiotaxis; los leucocitos "saben a dónde ir" gracias a los agentes quimiotácticos, los cuales a su vez causan la activación leucocitaria.
Los leucocitos ya activados cumplirán su función principal, eliminar al agente agresor del foco inflamatorio mediante la fagocitosis, que se dará en tres etapas, el reconocimiento y unión de partículas, interiorización con formación de vacuola fagocítica, y muerte o degradación del material patógeno ingerido.
Como ya se indicó este tipo de inflamación es una reacción rápida, por lo cual su cese también es rápido cuando el agente lesivo es eliminado y los mecanismos antiinflamatorios finalizan el proceso.
La inflamación puede restituirse al completo estado de normalidad solamente si se elimina el agente causal, se reabsorbe totalmente el exudado y se regeneran los tejidos destruidos. Este proceso dependerá del grado de respuesta de cada organismo a los mediadores químicos, y se podrán evidenciar tres posibles resultados del mismo:
Resolución completa.
Curación por reemplazo de tejido conectivo (fibrosis).
Progresión a una inflamación crónica.1,4,6,8,9
El proceso inflamatorio descrito corresponde más que todo a una inflamación aguda. En la inflamación crónica las características más importantes son:
Infiltrado celular compuesto por macrófagos, linfocitos y células plasmáticas.
Importante destrucción tisular.
Formación de tejido fibroso y angiogénesis (proliferación de pequeños vasos sanguíneos) prevalece sobre exudado de líquidos.
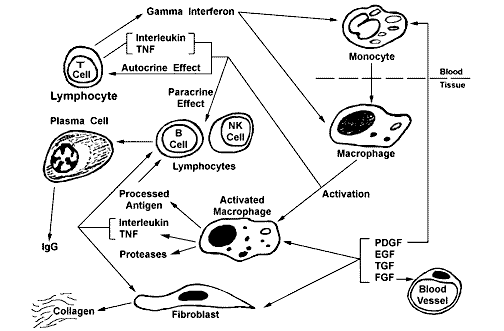
Los macrófagos son derivados de los monocitos del torrente sanguíneo, los cuales, al igual que los neutrófilos en la inflamación aguda, son inducidos a migrar de la luz de los vasos hasta el foco de la inflamación, por acción de los factores quimiotácticos. Estos macrófagos se activan gracias a citocinas producidas por las células T o por otros factores de origen no inmunitario. Este grupo celular será el de acumulación más persistente en la inflamación crónica.
Otras células que interfieren en este cuadro inflamatorio son los linfocitos y los eosinófilos. Las células cebadas están distribuidas por los tejidos conjuntivos y están presentes tanto en inflamación aguda como en la crónica.
Una forma específica de inflamación crónica es la inflamación granulomatosa, como reacción inflamatoria distintiva, la cual consiste en la presencia de granulomas. Los granulomas son focos microscópicos que se caracterizan por la presencia de agregados de macrófagos transformados en células epiteloides, que se refleja por un aplanamiento celular además de aumento de volumen, y a su vez estas células epiteloides están rodeadas por un collar de leucocitos mononucleares. Entre las causas para que se desencadene este tipo de inflamación, podemos mencionar causas bacterianas, como en el caso de tuberculosis y lepra, parasitarias, micóticas, por metales pesados, por presencia de cuerpos extraños, y por causas desconocidas.1,10